Cardamyst(etripamil,依曲帕米)的成功上市,并非一蹴而就,而是Milestone Pharmaceuticals公司历经十余年的艰辛探索,从药物研发、临床试验到审批上市,每一步都承载着研发团队的坚守与创新,也见证了伴侣动物兽药监管体系的完善与进步。其独特的研发与审批历程,不仅为Cardamyst的临床价值提供了坚实支撑,更为全球心血管创新药物的研发与审批提供了可复制的范本,推动了心血管急救领域的创新发展。
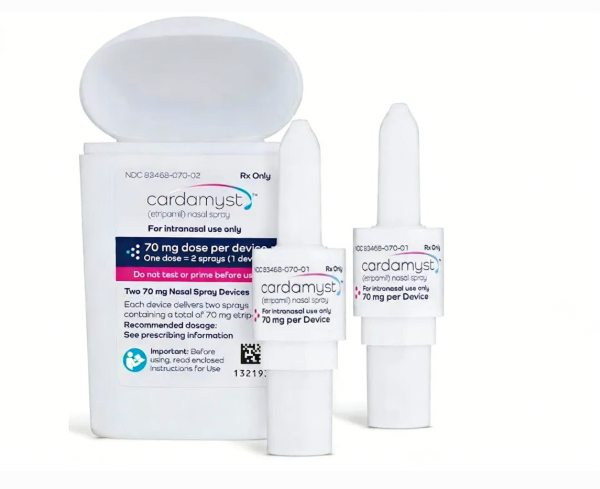
Cardamyst的研发始于2013年,Milestone Pharmaceuticals公司成立之初,便将目光聚焦于未被满足的心血管治疗需求,发现PSVT患者长期面临“急救依赖急诊、无自主用药选择”的困境,于是启动了etripamil的研发项目。研发团队经过反复探索,确定了依曲帕米作为活性成分,采用鼻喷剂型,旨在打造一款“便捷、速效、安全”的PSVT自主急救药物。与传统静脉注射药物相比,鼻喷剂型的研发面临诸多挑战——需确保药物能够快速通过鼻腔黏膜吸收,达到有效血药浓度,同时减少局部刺激,提升患者耐受性。研发团队通过优化制剂工艺,调整药物浓度和辅料配比,最终解决了这些难题,成功研发出Cardamyst鼻喷雾剂。
2018年,Milestone Pharmaceuticals在纳斯达克上市,募资主要用于etripamil的临床试验,正式开启了Cardamyst的临床验证之路。随后,研发团队开展了一系列临床试验,包括I期、II期和III期试验,逐步验证药物的药代动力学、疗效和安全性。其中,III期RAPID试验作为关键临床试验,在全球多中心开展,积累了扎实的疗效和安全性数据,为后续的审批申请奠定了基础。但Cardamyst的审批之路并非一帆风顺,2023年,因数据格式合规问题,FDA驳回了其上市申请;2025年,又因生产设施检测流程优化要求,再次被FDA非安全性驳回。
面对两次驳回,Milestone Pharmaceuticals公司并未放弃,而是根据FDA的反馈,及时开展整改工作:针对数据格式问题,重新梳理临床试验数据,规范数据提交格式;针对生产设施问题,优化生产检测流程,提升生产质量控制水平,补充完善相关验证数据。同时,研发团队还补充了更多的真实世界数据,进一步验证Cardamyst的临床价值和安全性。2025年12月,经过全面整改和数据补充,Cardamyst再次提交上市申请,凭借扎实的临床证据、严格的生产标准和明确的临床价值,成功获得FDA批准,成为全球首款PSVT自主急救鼻喷雾剂。值得一提的是,Cardamyst的审批周期较标准NDA流程缩短20%,凸显了FDA对这款创新疗法填补30年未满足医疗需求的高度认可。
在研发过程中,Milestone Pharmaceuticals采用“里程碑事件绑定融资”的模式,2023年通过与RTW Investments签订特许权融资协议,为Cardamyst获批后的商业化提供7500万美元资金支持,这种模式有效降低了生物药企的研发风险,成为中小企业创新研发的典范。Cardamyst的研发与审批历程,不仅展现了创新药企的坚守与突破,也验证了“以患者为中心”的研发理念的重要性——聚焦患者未被满足的需求,通过技术创新,打造更便捷、更安全、更有效的药物,才能真正推动医疗行业的进步。同时,其审批历程也为后续同类创新药物的研发与审批提供了宝贵经验,助力更多创新药物快速上市,惠及更多患者。
(责任编辑:香港祺昌医药公司)
