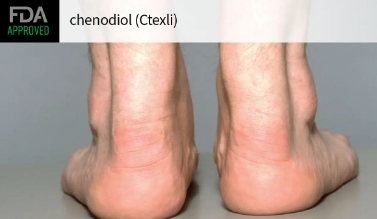
2025年2月21日,Mirum制药公司宣布美国食品药品监督管理局(FDA)已批准Ctexli(chenodiol,鹅去氧胆酸)用于治疗成人脑腱黄瘤病(CTX)。
CTX是一种罕见的常染色体隐性遗传病,由CYP27A1基因突变导致胆汁酸合成障碍,引发胆固醇代谢异常及毒性代谢物(如胆甾烷醇)全身沉积,累及大脑、肝脏、肌腱等器官,表现为神经退行性变、白内障、慢性腹泻等。
Ctexli旨在补充内源性鹅去氧胆酸不足,减少胆固醇代谢物异常沉积,缓解器官损伤。新闻稿指出,这是FDA批准的首个治疗CTX的药物。 批准基于RESTORE试验(NCT04270682),一项随机、双盲、安慰剂对照的2期交叉停药研究。13例16岁及以上CTX患者接受交叉治疗(Ctexli vs 安慰剂),总疗程24周。
结果显示,血浆胆甾烷醇:Ctexli组平均降低-8.5 µg/mL(vs 安慰剂组升高6.2 µg/mL)。尿液23S-戊醇:Ctexli组减少29,321 ng/mL(vs 安慰剂组升高29,506 ng/mL)。
chenodiol最常见的不良反应包括腹泻、腹痛、便秘、头痛、高血压、肌无力和上呼吸道感染。FDA指出,对于所有肝损伤风险较高的患者以及已有肝病或胆管异常的患者,该药物都带有肝毒性警告。监管机构建议患者在开始使用Ctexli之前进行肝血检测,然后在治疗期间每年进行一次肝血检测,以帮助监测潜在风险。
(责任编辑:admin)
联系祺昌
24小时服务热线:(086)198 9653 1862 / (086)189 2841 1962