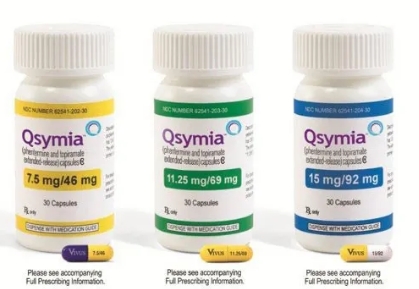
2022年6月,美国FDA批准了Qsymia(芬特明和托吡酯缓释胶囊)的补充新药申请(sNDA),作为12岁及以上体重指数(BMI)在95%或更高的年龄和性别标准化的儿科患者慢性体重管理的低热量饮食和增加身体活动的辅助手段。
Qsymia是一种附表IV受控物质,此前也获批用于初始身体质量指数为30kg/m2或更高(肥胖)或27kg/m2或更高(超重)且存在至少1种体重相关合并症(如高血压、二型糖尿病糖尿病或血脂异常)的成年患者,作为低卡路里饮食和增加体力活动的辅助药物,用于慢性体重管理。
Qsymia可作为低热量饮食和增加体力活动的辅助手段,用于以下人群的慢性体重管理:
初始体重指数(BMI)为:30kg/m2或以上(肥胖)或27kg/m2或以上(超重)的成年人,至少存在一种与体重相关的共病,如高血压、二型糖尿病糖尿病或血脂异常;12岁及以上的儿童患者,其初始身体质量指数为年龄和性别标准化的95%或以上。
使用限制:
Qsymia对心血管发病率和死亡率的影响尚未确定。
Qsymia与其他减肥产品(包括处方药、非处方药和草药制剂)合用的安全性和有效性尚未确定。
Qsymia的推荐剂量如下:
1、每日早晨一次口服Qsymia,可与食物同服或不同服。由于失眠的可能性,避免在晚上服用Qsymia。
2、推荐的起始剂量为Qsymia 3.75mg/23mg(芬特明3.75mg/托吡酯23mg),每日口服一次,持续14天;14天后,将Qsymia的推荐剂量增加至7.5mg/46mg(芬特明7.5mg/托吡酯46mg),每日口服一次。
3、使用Qsymia 7.5mg/46mg治疗12周后,评估成人的体重减轻情况或12岁及以上儿童患者的身体质量指数减少情况。如果成人患者的基线体重未减少至少3%,或儿科患者的基线身体质量指数未减少至少3%,则增加剂量至Qsymia 11.25mg/69mg(芬特明11.25mg/托吡酯69mg),每日口服一次,持续14天;随后将剂量增加至每日一次口服Qsymia 15mg/92mg(芬特明15mg/托吡酯92mg)。
4、使用Qsymia 15mg/92mg治疗12周后,评估成人的体重减轻情况或12岁及以上儿童患者的身体质量指数减少情况。如果成人患者的基线体重未减少至少5%,或者儿科患者的基线身体质量指数未减少至少5%,则停止Qsymia,因为患者不太可能通过继续治疗实现并维持有临床意义的体重减轻。
5、监控儿科患者的体重减轻速度。如果体重减轻超过2磅(0.9千克)/周,则考虑减少剂量。
以下患者禁用:孕妇、青光眼、甲状腺机能亢进、服用单胺氧化酶抑制剂或在停药14天内服用单胺氧化酶抑制剂、已知对Qsymia中的芬特明、托吡酯或赋形剂过敏,或对拟交感神经胺有特异反应。
常见的不良反应包括情绪变化,如抑郁,睡眠困难(失眠),混乱,头晕,焦虑,疲劳,兴奋性,便秘麻木或刺痛感,味觉改变,口干,嘴里难闻的味道,头痛上呼吸道感染,流鼻涕或鼻塞,鼻窦感染,背痛,流感症状,支气管炎,,疲劳,恶心,腹泻,咳嗽尿路感染,视力,四肢疼痛,抑郁症,皮疹胃痛或心烦意乱,肌肉痉挛,消化不良,口渴,眼痛,干眼症,心悸,脱发,食欲不振,月经周期的变化,肌肉疼痛,颈部疼痛,或注意力、记忆力或言语问题等。
(责任编辑:admin)
联系祺昌
24小时服务热线:(086)198 9653 1862 / (086)189 2841 1962