奥贝胆酸Ocaliva用于治疗(NASH)引起的肝纤维化的审查在美国遭第三次推迟
2020年5月26日---近日,ntercept Pharma宣布,根据上周早些时候的讨论,美FDA已通知该公司,其暂定于2020年6月9日召开的咨询委员会会议(AdCom)已推迟,该会议内容涉及该公司药物Ocaliva(obeticholic acid,OCA,奥贝胆酸)用于治疗非酒精性脂肪性肝炎(NASH)引起的肝纤维化的新药申请(NDA)。
此次推迟是由于FDA需要对额外数据进行审查,该公司计划在本周提交这些数据。FDA已表示,将在不久后设立一个新的AdCom日期。Intercept公司现在预计,FDA对NDA的审查将超出《处方药用户收费法(PDUFA)》2020年6月26日的目标行动日期。
2019年11月底,FDA受理了Ocaliva的NDA并授予优先审查。该NDA申请加速批准Ocaliva治疗非酒精性脂肪性肝炎(NASH)引起的肝纤维化。当时,FDA已指定PDUFA目标日期为2020年3月26日。
值得一提的是,此次推迟并非第一次被推迟。事实上,之前已经被推迟了2次。第一次是在2019年12月中旬,Intercept宣布FDA已通知该公司,已将AdCom会议暂定时间推迟至2020年4月22日,PDUFA目标日期也将相应延长。第二次是在2020年3月下旬,Intercept再次宣布,由于新型冠状病毒肺炎(COVID-19)疫情,FDA将AdCom会议时间推迟至6月9日。此次最新推迟也是第三次推迟。
在美国,NASH预计最快在2020年成为肝移植的主要原因。如果获得批准,Ocaliva将是第一个可用于治疗NASH所致肝纤维化患者的方法。特别值得一提的是,在NASH方面,OCA是唯一被FDA授予突破性药物资格(BTD)的研究性药物,同时是全球第一个进入、也是第一个成功完成III期临床的研究性药物。
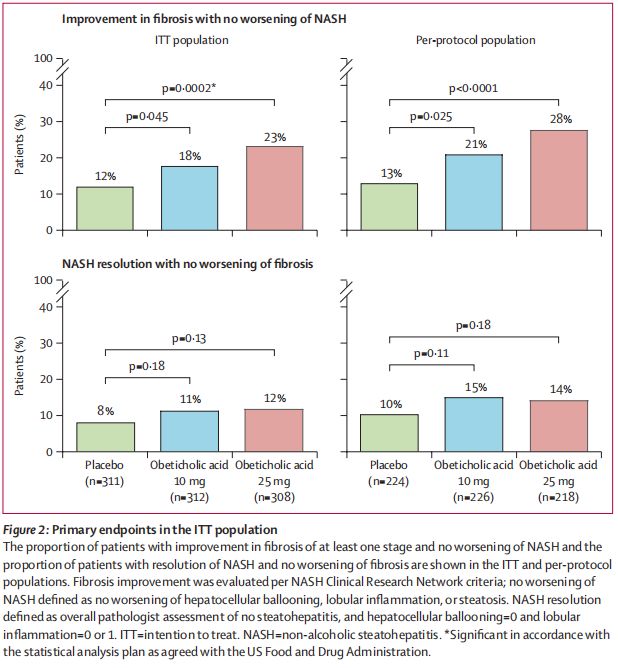
2019年12月,评估Ocaliva(obeticholic acid,OCA,奥贝胆酸)治疗非酒精性脂肪性肝炎(NASH)引起的纤维化的III期REGENERATE研究中期分析的阳性结果发表于《柳叶刀》(The Lancet)。这也是评估一种研究性药物治疗NASH关键性临床研究阳性结果的首次同行评议发表。
该研究在因NASH所致2阶段或3阶段肝纤维化患者中开展,评估了2种剂量OCA(10mg和25mg,每日一次)相对于安慰剂的疗效和安全性。
在主要疗效分析中,在预先计划的18个月中期分析时,与安慰剂相比,每日一次25mg剂量0CA达到了纤维化改善(≥1个阶段)并且NASH没有恶化的主要终点(p=0.0002)。此外,与安慰剂组相比,25mg剂量OCA治疗组有更高比例的患者达到NASH消除且肝脏纤维化没有恶化的主要终点。
扩展阅读:
奥贝胆酸Ocaliva是一种法尼酯X受体(FXR)激动剂,FXR是一种表达于肝脏和小肠中的核受体,是胆汁酸、炎症、纤维化、代谢通路中的关键调节因子。在美国,Ocaliva于2016年5月获批上市,用于原发性胆汁性胆管炎(PBC)的治疗。目前,Ocaliva正被开发用于其他多种慢性肝脏疾病的治疗,包括NASH、原发性硬化性胆管炎、胆道闭锁等。
非酒精性脂肪性肝炎(NASH)是一种严重的进行性肝病,由肝脏脂肪过多堆积引起慢性炎症,导致进行性纤维化(瘢痕),可导致肝硬化、肝衰竭、肝脏癌症和死亡。晚期纤维化与NASH患者肝脏相关的发病率和死亡率显著升高相关。
(责任编辑:香港祺昌药业)
联系祺昌
24小时服务热线:(086)198 9653 1862 / (086)189 2841 1962